Spletna revija za znanstvenike, strokovnjake
in nevroznanstvene navdušence
Naslovnica Članki Intervjuji Mnenja Zdravje Korenine eSinapsa Številke ![]()
Ondinino prekletstvo ali sindrom prirojene centralne hipoventilacije
letnik 2016, številka 11
uvodnik
Grega Repovš
članki
Mara Bresjanac
Kako ultrazvok odpira pot v možgane
Kaja Kolmančič
Kako je epigenetika spremenila nevroznanost
Metka Ravnik Glavač
Ondinino prekletstvo ali sindrom prirojene centralne hipoventilacije
Katja Pavšič, Barbara Gnidovec Stražišar, Janja Pretnar Oblak, Fajko F. Bajrović
Motnje ravnotežja otrok in odraslih
Nejc Steiner, Saba Battelino
Zika virus in magnetnoresonančna diagnostika nepravilnosti osrednjega živčevja pri plodu
Rok Banko, Tina Vipotnik Vesnaver
mnenje
kolofon
letnik 2016, številka 11
»Obljubil si mi zvestobo in ljubezen z vsakim svojim dihom. Obljubo si prelomil, torej naj bo tako. Odslej boš moral misliti na vsak svoj dih. Če boš zaspal, boš pozabil dihati!« Tako je prelepa vodna nimfa Ondina preklela svojega ljubimca, ko ji je prenehal biti zvest. Vsakdo je že kdaj pomislil na čudež narave, ki nas ohranja pri življenju vsak trenutek in nam omogoča dihanje tudi, ko spimo. Le redki pa vedo, da obstajajo ljudje s prirojeno boleznijo, zaradi katere v spanju resnično »pozabijo dihati«.
Sindrom prirojene centralne hipoventilacije (SPCH), včasih znan kot Ondinino prekletstvo, je redka genetska bolezen avtonomnega živčevja, ki predvsem v spanju, vodi v nezadostno dihanje oz. hipoventilacijo1.
Bolezen je leta 1970 prvič opisal dr. Robert Mellins s sodelavci, pri novorojenčku, ki je kmalu po rojstvu začel nezadostno dihati, predvsem med hranjenjem in spanjem2. Navdih za poimenovanje bolezni so črpali iz francoske drame Ondine iz leta 19383. Da bi se izognili stigmatizaciji bolnikov, se izraz Ondinino prekletstvo danes opušča in se uveljavlja strokovno poimenovanje – sindrom prirojene centralne hipoventilacije. Prvemu opisu je sledilo več opisov drugih primerov SPCH, širša ozaveščenost pa je sledila prvim večjim raziskavam v 90-tih letih, ko je Ameriško torakalno združenje (angl. American Thoracic Society) objavilo prvi obširnejši opis bolezni in njenega zdravljenja. V 21. stoletju se raziskave na tem področju nadaljujejo, tako na molekularno-genetski kot na klinični ravni4.
Leta 2003 so znanstveniki odkrili, da je za nastanek SPCH odgovorna mutacija v genu PHOX2B na četrtem kromosomu, ki kodira transkripcijski faktor, odgovoren za razvoj avtonomnega živčevja. Po podatkih iz leta 2009 so z genetskim testiranjem potrdili približno tisoč primerov SPCH v svetu1 4. Verjetno pa je prevalenca bolezni še višja, saj v primerih blažje oblike bolezni ali v primerih zgodnje smrti novorojenčka pogosto ostane neprepoznana.
Genetika SPCH
Gen PHOX2B na določenem mestu (eksonu številka 3) normalno vsebuje 20 ponovitev zapisa za aminokislino alanin. V 90 % primerov se zaradi mutacije v genu PHOX2B poveča število ponovitev zapisa za alanin z 20 na 24 do 33, pri čemer več ponovitev zapisa za alanin običajno pomeni težji klinični potek bolezni1. Le v 10 % pa mutirani gen PHOX2B ne vsebuje čezmernih ponovitev zapisa za alanin, temveč t. i. mutacije s premikom bralnega okvira DNK, nesmiselne in drugačnosmiselne mutacije (angl. frameshift, nonsense, missense mutations). Te vrste mutacij so prav tako povezovali s hujšim potekom bolezni1.
Za nastanek SPCH zadostuje mutacija gena PHOX2B le na enem alelu, torej le na enem izmed dveh četrtih kromosomov. Bolezen tako izkazuje dominanten način dedovanja in se na potomce prenese v 50 % primerov. Kljub temu večina mutacij ni podedovanih, ampak se pojavijo de novo med razvojem zarodka. Le v 5 do 10 % primerov je mutacija prisotna pri starših, ki pa imajo večinoma blago, pogosto do tedaj neprepoznano obliko bolezni1.
Fiziologija dihanja
Temeljna naloga dihanja je izmenjava dihalnih plinov – vdihavanje kisika, ki je nujen v telesnih presnovnih procesih, in izdihavanje ogljikovega dioksida, ki nastane kot odpadni produkt presnove6. Dihamo s pomočjo dihalnih mišic prsnega koša, glavna dihalna mišica pa je trebušna prepona. Krčenje trebušne prepone in ostalih dihalnih mišic je pod nadzorom osrednjega živčevja. V predelu možganov, imenovanem možgansko deblo, se nahajajo avtonomni dihalni centri, v katerih se nahajajo živčne celice, ki – podobno kot t. i. »pacemakerske« celice v srcu – nenehno v ritmičnem vzorcu prožijo električne signale in jih preko hrbtenjače in motoričnih perifernih živcev oddajajo dihalnemu mišičju. Tako nastane osnovni vzorec dihanja s fazo vdiha in izdiha, hitrost in globino dihanja pa morajo dihalni centri v možganskem deblu prilagoditi potrebam organizma oz. spremembam ravni kisika in ogljikovega dioksida v krvi. Za optimalno delovanje biokemijskih procesov v telesu je namreč izredno pomembno, da je delni tlak teh dveh plinov v krvi ves čas v ozko omejenem območju. Spremembe v delnih tlakih kisika in ogljikovega dioksida zaznavajo kemoreceptorne celice, ki se nahajajo v velikih arterijah, ki vodijo iz srca (aortni lok, razcepišče karotidnih arterij) in v možganskem deblu. Če se poveča delni tlak ogljikovega dioksida ali zmanjša delni tlak kisika v krvi, začnejo kemoreceptorne celice pospešeno spodbujati dihalni center v možganskem deblu, ki posledično, pospešeno, oddaja živčne signale dihalnim mišicam. Tako se dihanje poglobi in pospeši in se izdiha odvečni ogljikov dioksid ter vdiha primanjkljaj kisika. Tovrstno uravnavanje dihanja se odvija popolnoma samodejno, neodvisno od naše volje6.
Patofiziologija SPCH
Gen PHOX2B ima ključno vlogo v normalnem razvoju avtonomnega živčevja, ki je pomembno za delovanje številnih telesnih funkcij, med drugim tudi za uravnavanje dihanja1 5. Zaradi mutacije gena PHOX2B je pri bolnikih s SPCH sistem za samodejno dihanje slabše razvit, zato je odziv kemoreceptornih celic na spremembe dihalnih plinov v krvi slabši4. Posledično pride do plitvejšega in počasnejšega dihanja oz. hipoventilacije, ki vodi do porasta delnega tlaka ogljikovega dioksida in padca delnega tlaka kisika v krvi. Hipoventilacija se običajno poslabša v spanju. Takrat se namreč že pri zdravih ljudeh zmanjša odzivnost kemoreceptorjev in upočasni dihanje, kar ob okvari kemoreceptorjev vodi v hipoventilacijo ali celo v prekinitve dihanja (apneje). V budnosti pa so kemoreceptorji bolj občutljivi, zato se dihanje izboljša. Poleg tega je dihanje v budnosti pod vplivom višjih možganskih funkcij, npr. pod vplivom sistema za hoteni nadzor dihanja, ki se nahaja v velikih možganih in lahko uravnava dihanje neodvisno od sistema za avtomatični nadzor dihanja. Sistem za hoteni nadzor dihanja je pomemben, kadar želimo poglobiti dihanje ali zaustaviti dih med govorom, petjem ali igranjem pihalnih instrumentov4. Bolniki s SPCH imajo sistem za hoteni nadzor dihanja primerno razvit in lahko v budnosti hoteno dihajo primerno. Težavo v budnosti pa predstavljajo monotone aktivnosti, kot so branje, gledanje televizije, igranje računalniških igric ipd., ko ti bolniki lahko »pozabijo« dihati. Zaradi nerazvitega subjektivnega občutka za pomanjkanje diha se ob tem ne začnejo dušiti, temveč pomodrijo, lahko se tudi onesvestijo in celo umrejo4 5 7 (Slika 2).
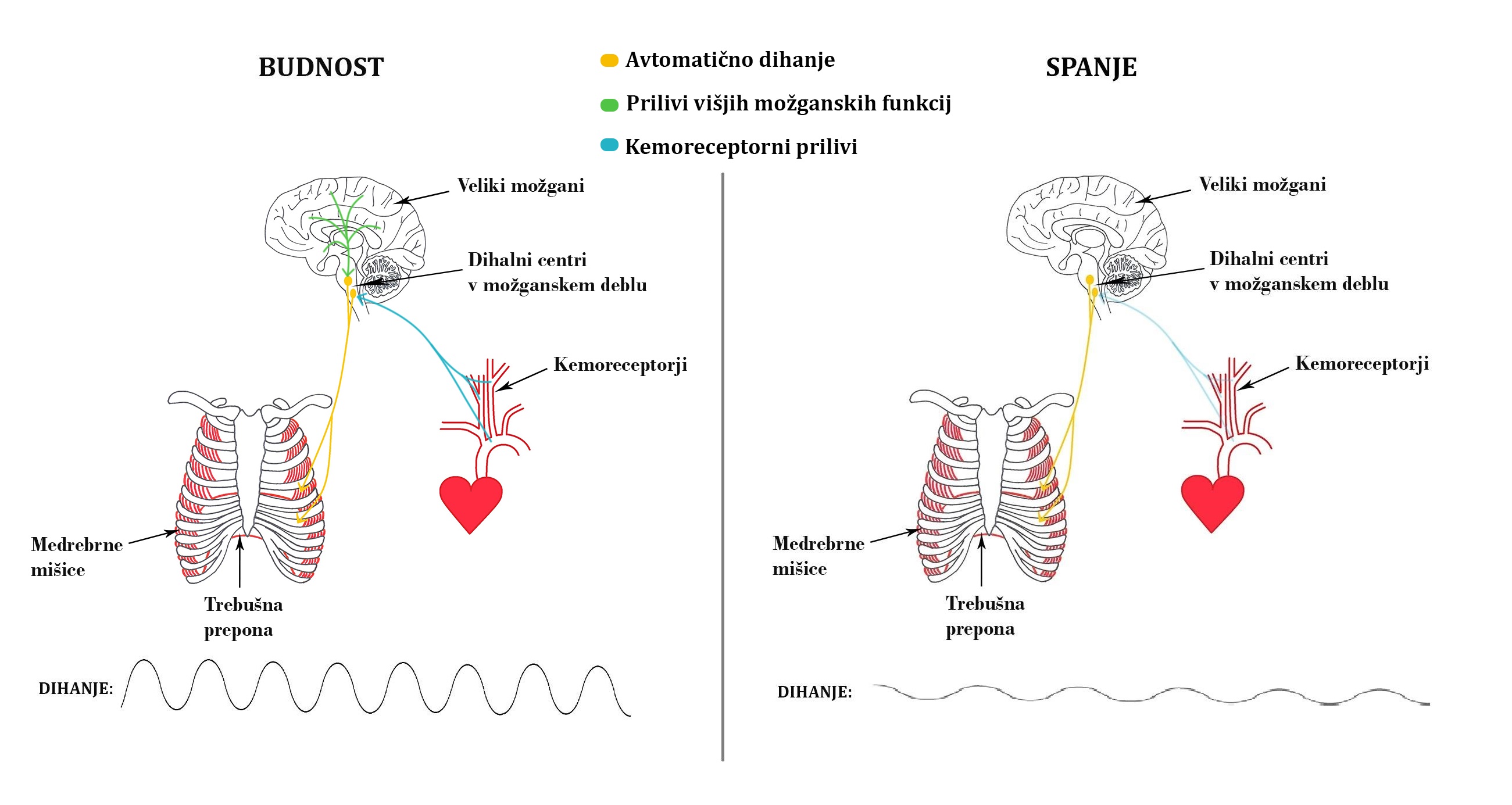
Slika 2. Shematični prikaz uravnavanja dihanja v spanju in budnosti.
Dihanje v budnosti je pod nadzorom sistema za avtomatično dihanje, ki je pod vplivom višjih možganskih funkcij (npr. sistema za hoteni nadzor dihanja) in kemoreceptornih prilivov. V spanju prilivi višjih možganskih funkcij upadejo in se občutljivost kemoreceptornega sistema zmanjša. Dihanje v spanju tako že pri zdravih ljudeh postane počasnejše in plitvejše. Prirojena okvara kemoreceptorjev v sklopu sindroma prirojene centralne hipoventilacije pa povzroči še dodatno upočasnitev dihanja v spanju ter lahko vodi v hudo hipoventilacijo in prekinitve dihanja v spanju.
Klinična slika SPCH
Stopnja prizadetosti avtonomnega živčevja je lahko pri bolnikih s SPCH različna in je odvisna od resnosti okvare gena PHOX2B1 8. V skladu s tem je lahko tudi klinični potek bolezni različno težek. V primerih blažje okvare avtonomnega živčevja je prisotna le blaga hipoventilacija v spanju in normalno dihanje v budnosti, v primerih težje okvare pa se klinična slika slabša in v najhujši obliki obsega popolno odpoved dihanja v spanju in hudo hipoventilacijo v budnosti. Težje oblike se po navadi izrazijo takoj po rojstvu s hudo dihalno stisko in ti bolniki običajno potrebujejo dosmrtno stalno mehanično podporo dihanju. Nasprotno pa se blažje oblike lahko pokažejo šele več mesecev ali let po rojstvu, lahko šele v odrasli dobi. V teh primerih se bolezen večinoma izrazi v stanjih z zmanjšano dihalno rezervo, kot je hujša pljučnica, ali pa po operacijah v splošni anesteziji, ki dihalne centre upočasni in zato bolniki dlje časa ne dihajo zadovoljivo.
Ker je gen PHOX2B vpleten v razvoj celotnega avtonomnega živčevja, so pri bolnikih s SPCH pogosto prisotne tudi druge motnje v delovanju avtonomnega živčevja1 8. Pojavljajo se motnje srčnega ritma, motnje v uravnavanju telesne temperature s čezmernim potenjem, motnje zeničnih reakcij, motnje gibanja požiralnika in motnje gibanja črevesja oz. Hirshprungova bolezen. Pogostejši so tudi tumorji živčnih celic (t. i. primitivni nevroektodermalni tumorji), ki so lahko benigni ali maligni. Moten je lahko tudi razvoj velikih možganov s posledično slabšim kognitivnim delovanjem. Ni še povsem jasno, ali je okvara velikih možganov posledica same mutacije v genu PHOX2B ali le zmanjšane ravni kisika v krvi. Podobno kot motnje dihanja se tudi motnje drugih funkcij avtonomnega živčevja pogosteje pojavljajo pri mutacijah z večjim številom ponovitev zapisa za alanin ter pri mutacijah, pri katerih ne gre za povečano število ponovitev zapisa za alanin.
Zdravljenje SPCH
Vzročnega zdravljenja SPCH še ne poznamo. Zdravljenje temelji na mehanični podpori dihanju ter odkrivanju in zdravljenju drugih motenj delovanja avtonomnega živčevja. Zaradi kompleksnosti in številnih spremljajočih zapletov je obravnava teh bolnikov zahtevna, zato jih vodimo v specializiranih centrih, ki so usmerjeni v vodenje bolnikov s SPCH1 8.
Zdravljenje z mehanično podporo dihanju lahko poteka na različne načine1 8. Večinoma je podpora dihanju potrebna le ponoči, pri težjih oblikah pa tudi čez dan. V prvih letih življenja, ko so zgornje dihalne poti nagnjene k sesedanju, večinoma uporabljajo mehanično ventilacijo preko traheostome (kirurška odprtina na vratu s povezavo v sapnik). V kasnejših letih življenja pa lahko preidejo na neinvazivne načine mehanične ventilacije preko različnih obraznih ali nosnih mask. Poseben način spodbujanja dihanja pa predstavlja tudi kirurška vstavitev električnega spodbujevalnika trebušne prepone.
Izrednega pomena je tudi izobraževanje staršev, ki se morajo natančno seznaniti z boleznijo in metodo mehanične ventilacije, ki je bo otrok deležen na domu1 8. Starši morajo znati namestiti in uporabljati aparat za mehanično ventilacijo ter v primeru nezadostnega dihanja le-to prepoznati in primerno ukrepati. Pomembno je tudi, da so otroci s SPCH stalno nadzorovani. Podnevi je treba paziti, da otrok ne zaspi nenadzorovano, saj lahko v tem primeru preneha dihati. V primeru monotonih aktivnosti pa je treba otroka aktivno spodbujati k dihanju.
Smrtnost je pri bolezni v prvih mesecih življenja visoka in po ocenah znaša od 20 do 40 %5. Kljub temu pa lahko v primeru zgodnje prepoznave bolezni, dobre oskrbe v domačem okolju in rednega spremljanja v specializiranih centrih bolniki s SPCH živijo polno življenje, sposobni so se šolati v rednem programu, zaključiti študij in se zaposliti1. V prihodnosti pa morda lahko pričakujemo razvoj terapevtskih metod, s pomočjo katerih bi lahko vplivali na aktivnost avtonomnega živčevja. Na živalskih modelih namreč že potekajo raziskave različnih snovi (npr. derivatov progesterona), ki bi lahko izboljšale občutljivost kemoreceptorjev, in morda v daljni prihodnosti bolnikom s SPCH omogočile življenje brez potrebe po mehanični ventilaciji, ali pa bi to potrebo vsaj zmanjšale5.
-
___
-
Weese-Mayer DE, Berry-Kravis EM, Ceccherini I, Keens TG, Loghmanee DA, Trang H. An Official ATS Clinical Policy Statement: Congenital Central Hypoventilation Syndrome. Am J Respir Crit Care Med. 2010; 181 (6): 626–44. ↩
-
Mellins RB, Balfour HH Jr., Turino GM, Winters RW. Failure of automatic control of ventilation (Ondine’s curse). Report of an infant born with this syndrome and review of the literature. Medicine (Baltimore). 1970; 49: 487–504. ↩
-
Jean Giraudoux. Ondine. Le Livre De Poche; 1938 ↩
-
Weese-Mayer DE, Rand CM, Berry-Kravis EM, Jennings LJ, Loghmanee DA, Patwari PP, et al. Congenital central hypoventilation syndrome from past to future: Model for translational and transitional autonomic medicine. Pediatr Pulmonol. 2009; 44 (6):521–35. ↩
-
Sowho M, Amatoury J, Kirkness JP, Patil SP. Sleep and Respiratory Physiology in Adults. Clin Chest Med. 2014; 35 (3): 469-81. ↩
-
Ramanantsoa N, Gallego J. Congenital central hypoventilation syndrome. Respir Physiol Neurobiol. 2013; 189 (2): 272–9. ↩
-
Harper RM, Kumar R, Macey PM, Harper RK, Ogren JA. Impaired neural structure and function contributing to autonomic symptoms in congenital central hypoventilation syndrome. Front Neurosci. 2015; 9: 415. ↩
-
Trang H, Brunet JF, Rohrer H, Gallego J, Amiel J, Bachetti T, et al. Proceedings of the fourth international conference on central hypoventilation. Orphanet J Rare Dis. 2014; 9: 194. ↩
Katja Pavšič, dr. med.1, asist. dr. Barbara Gnidovec Stražišar, dr. med.2, doc. dr. Janja Pretnar Oblak, dr. med.1, prof. dr. Fajko F. Bajrović, dr. med.1
1 Nevrološka klinika, Univerzitetni klinični center Ljubljana
2 Otroški oddelek, Splošna bolnišnica celje
Recenzirala
izr. prof. dr. Leja Dolenc Grošelj, dr. med.
Klinični inštitut za klinično nevrofiziologijo
Nevrološka klinika
Univerzitetni klinični center Ljubljana
Uroš Krivec, dr. med.
Služba za pljučne bolezni
Pediatrična klinika
Univerzitetni klinični center Ljubljana
Prispelo: 2. junij 2016
Sprejeto: 13. junij 2016
Objavljeno: 11. julij 2016
