Spletna revija za znanstvenike, strokovnjake
in nevroznanstvene navdušence
Naslovnica Članki Intervjuji Mnenja Zdravje Korenine eSinapsa Številke ![]()
Zunajcelični vezikli kot prenašalci zdravilnih učinkovin preko krvno-možganske prepreke
letnik 2020, številka 19
uvodnik
članki
Ob mednarodnem dnevu znakovnih jezikov
Anka Slana Ozimič
Teorija obetov: kako sprejemamo tvegane odločitve
Nastja Tomat
Sara Fabjan
Matjaž Deželak
Nina Stanojević, Uroš Kovačič
Od človeških nevronov do možganskih organoidov – nova obzorja v nevroznanosti
Vesna M. van Midden
Splošna umetna inteligenca ali statistične jezikovne papige?
Kristijan Armeni
Zunajcelični vezikli kot prenašalci zdravilnih učinkovin preko krvno-možganske prepreke
Saša Koprivec
Matjaž Deželak
kolofon
letnik 2020, številka 19
Kljub hitremu napredku znanosti številne bolezni centralnega živčnega sistema ostajajo uganka. V primerjavi s pojavom novih metod zdravljenja število bolnikov z nevrodegenerativnimi obolenji in možganskim rakom v zadnjih letih raste eksponentno. Pomemben faktor predstavlja krvno-možganska prepreka, ki možgane ščiti pred negativnimi vplivi, hkrati pa onemogoča vnos zdravil in zmanjšuje učinkovitost obstoječih terapij. Znanost je vedno usmerjena v iskanje novih tehnologij, ki bi omogočile ustrezno zdravljenje s čim manj stranskimi učinki, in tako je tudi pri iskanju novih možnosti prenosa zdravilnih učinkovin preko krvno-možganske prepreke.
Število bolnikov z boleznimi centralnega živčnega sistema (CŽS) zaradi staranja prebivalstva narašča, razvoj novih zdravil in terapij pa temu trendu rasti ne sledi 1. Nevrodegenerativna obolenja (med drugimi so bolj splošno prepoznavne Alzheimerjeva, Parkinsonova in Huntingtonova bolezen) imajo velik vpliv na zmanjšanje kvalitete življenja, bolniki predstavljajo tudi finančno in socialno breme 2. Po podatkih Svetovne zdravstvene organizacije (angl. World Health Organization) so bile nevrodegenerativne bolezni v letu 2016 peti najpogostejši vzrok smrti 3. Velik del raziskav je usmerjen v iskanje učinkovitih pristopov za zdravljenje bolezni CŽS. Velik korak naprej predstavljajo novejše raziskave uporabe zunajceličnih veziklov. Vezikli, ki prihajajo iz CŽS, nam posredujejo informacije o samih živčnih celicah. Vezikli, ki jih pošljemo nazaj v CŽS, pa omogočajo ciljni vnos učinkovin do celic živčnega sistema 4. Ko bomo razvili ustrezne podporne tehnologije, bo sposobnost zunajceličnih veziklov za prenos zdravil preko bioloških preprek revolucionarno vplivala na zdravljenje nevroloških bolezni 2.
Vloga krvno-možganske prepreke
Krvno-možganska prepreka (KMP) deluje kot zapornica, ki zaradi tesnih medceličnih stikov onemogoča prosti pretok snovi med možgani in perifernim krvnim obtokom in tako sodeluje pri vzdrževanju homeostaze CŽS 5 6. Sestavljena je iz tesnega prepleta kapilar, ki jih gradijo endotelijske celice skupaj s periciti, astrociti, tesnimi stiki, nevroni in bazalno membrano (slika 1) 1. Zaradi zmanjšane prepustnosti so možgani zaščiteni pred toksičnimi snovmi, ki so lahko prisotne in krožijo po krvnem obtoku, s terapevtskega vidika pa ta lastnost zelo otežuje vnos zdravil 2.
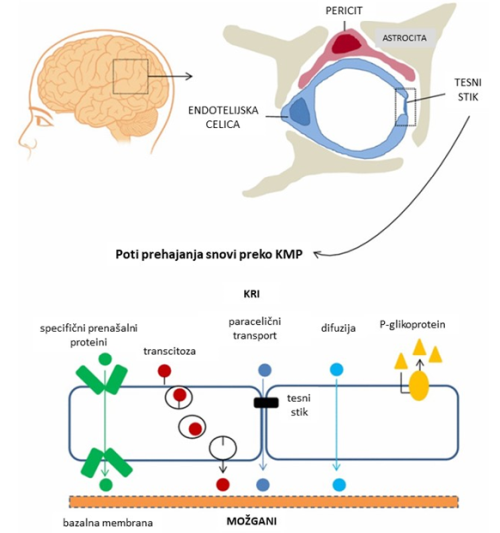
Slika 1. Poti prehajanja molekul preko krvno-možgansko prepreko (KMP). KMP sestavljajo tesne možganske kapilare, ki jih tvorijo endotelijske celice, pericite, astrociti, tesni stiki med temi celicami, nevroni in bazalna membrana. Ioni in drugi topljenci, ki so dovolj majhni, se lahko poslužujejo koncentracijskega gradienta ter preko KMP prehajajo s pasivno difuzijo skozi ozek medcelični prostor med dvema celicama (tj. paracelični prenos snovi). Transcelični transport vključuje različne mehanizme prehajanja snovi, npr. pasivno difuzijo preko celice, delovanje celičnih prenašalcev ali transcitoza. Na prepustnost KMP vpliva še delovanje različnih aktivnih prenašalcev, kot je P-glikoprotein, ki omogočajo prenos lipofilnih snovi (prirejeno po 2).
KMP je dinamična struktura, ki se nenehno prilagaja fiziološkim spremembam v možganih (mikrookolje) in signalom, ki izhajajo iz zunanjega okolja 5. Molekule lahko prečkajo KMP na dva načina. KMP lahko prosto prehajajo le molekule, ki so topne v lipidih in manjše od 400 Da. Takšne majhne molekule (npr. ioni) lahko izkoristijo paracelične transportne poti in prehajajo v CŽS skozi špranje med sosednjimi celicami. Druga možnost transporta je prehajanje preko celic, kjer se molekule poslužujejo različnih načinov prenosa – difuzije, prenosa preko transportnih proteinov ali transcitoze. Fizikalno-kemijske lastnosti molekule določajo ali in na kakšen način bo ta prestopila mejo KMP. Patološka bolezenska stanja CŽS, kot so možganska kap, sladkorna bolezen, hipertenzijska encefalopatija, AIDS, multipla skleroza ter Parkinsonova in Alzheimerjeva bolezen, povzročijo moteno prepustnost KMP 1.
Pristopi za vnos zdravil v CŽS
Preizkušajo se številne metode vnosa zdravil preko KMP. Virusni vektorji posedujejo naravno sposobnost vnosa nukleinskih kislin v celice. Raziskovalci se že več desetletij ukvarjajo z vnosom v virusne vektorje vključenih genov preko KMP za zdravljenje bolnikov z nevrološkimi obolenji. Vendar je proizvodnja težavna in draga, terapija z virusi pa vzbuja varnostne pomisleke, tudi zaradi številnih smrti bolnikov v kliničnih testiranjih 7. Nanodelci omogočajo ciljano dostavo zdravil do možganov, vendar sami po sebi niso vedno sposobni prečkati KMP, temveč delujejo tako, da zdravilu omogočijo daljši čas zadrževanja na ciljnem mestu 8. Tudi liposomi predstavljajo vsestranski in fleksibilen sistem, ki ima številne prednosti (ustrezna zaščita zdravila, ki ga prenašamo, obstojnost v krvnem sistemu, biorazgradljivost, nizka toksičnost). Ker niso endogenega izvora, obstaja verjetnost sprožitve imunskega sistema preko aktivacije sistema komplementa ali fagocitoze s strani makrofagov 9. Še en pristop uporablja obstoječe transportne sisteme – vezavo zdravil na ciljne aminokisline, ki lahko aktivno prečkajo KMP – vendar je tak pristop uporaben samo za majhne molekule. Z določenimi neinvazivnimi tehnikami (ultrazvok) lahko olajšamo prehod zdravil preko KMP, obstaja pa nevarnost toksičnosti za zdravo možgansko tkivo 4. V zadnjih letih se intenzivno raziskuje možnost uporabe zunajceličnih veziklov, natančneje eksosomov, za ciljni vnos zdravil preko KMP.
Kaj so zunajcelični vezikli?
Termin zunajcelični vezikli zajema heterogeno skupino veziklov, ki jih izločajo celice (so telesu avtologni) in prenašajo raznovrsten celični tovor bodisi v bližnje mikrookolje bodisi do oddaljenih mest s pomočjo obtočilnega sistema 6. Ločimo eksosome, mikrovezikle in apoptotska telesca (slika 2). Glede na izvor (progenitorska celica) se vezikli med seboj razlikujejo, saj vsebujejo specifične citosolne proteine, lipide in genetski material (mRNA, miRNA, druge majhne nekodirajoče RNA, gDNA izvorne celice). Na njihovo vsebino vplivajo tudi zunanji dejavniki, katerim je celica izpostavljena v času nastanka vezikla, zato se le-ti razlikujejo tudi, če izvirajo iz iste skupine celic (npr. izpostavljenost toksičnim snovem, hipoksični pogoji ipd.) 10. Eksosomi so podskupina zunajceličnih veziklov, ki se od drugih najbolj razlikujejo po svoji velikosti. Merijo nekje od 30 do 100 nm, kar pomeni, da sodijo v velikostni razred nanodelcev 12. Pod elektronskim mikroskopom je vidna značilna morfologija sploščene krogle, ki je omejena z lipidnim dvoslojem 11. O njihovi vlogi v telesu še ne vemo vsega, jasno pa je, da imajo pomembno vlogo v medcelični komunikaciji, tako v normalni pogojih kot v določenih patoloških stanjih 9.
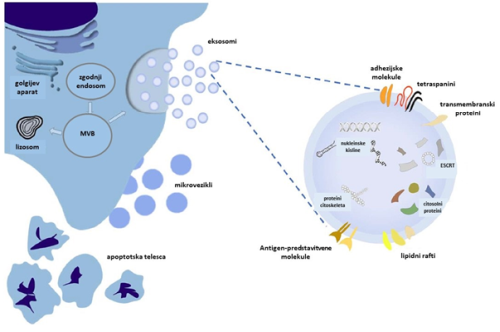
Slika 2. Grafična ponazoritev biogeneze in sestave zunajceličnih veziklov. Termin zunajcelični vezikli zajema različne vrste veziklov – eksosome (30–150 nm), mikrovezikle (50nm–1 µm) in apoptotska telesca (do 5 µm). Eksosomi, ki so najbolje preučeni, nastanejo z notranjim brstenjem t. i. multivezikularnih telesc (MVB, angl. MultiVesicular Bodies). MVB se ob stiku z lizosomom razgradijo ali pa ob zlitju s plazemsko membrano v zunajcelični prostor sproščajo eksosome. Mikrovezikli so večji kot eksosomi in nastanejo z brstenjem celične membrane. Največja so apoptotska telesca, nastajajo pa kot odpadni/izvrženi material celic, ki vstopajo v cikel programirane celične smrti ali apoptoze. Eksosomi so bogati z lipidnimi rafti (flotilin-1, holesterol), nukleinskimi kislinami (DNA in RNA) in številnimi proteini (adhezijske molekule, tetraspanini, citosolni proteini, komponente endosomalnih kompleksov, potrebnih za transport-ESCRT) (prirejeno po 11).
Zaradi unikatnih lastnosti se raziskujejo možnosti uporabe eksosomov kot bioloških označevalcev za zgodnjo in neinvazivno diagnostiko ali prognozo bolezni CŽS 12. Ker izvirajo iz celic, se lahko izognejo imunskemu sistemu in fagocitozi. Ciljne celice jih privzamejo, zato so sposobni svoj tovor dostaviti direktno v citoplazmo, s čimer se znotraj receptorske celice izognejo delovanju lizosomov ali drugih poti razgradnje 9.
Raziskave nakazujejo, da imajo pri boleznih CŽS eksosomi dvojno vlogo. Po eni strani celice eksosome uporabljajo, da iz citoplazme izločajo toksične proteine in agregate, po drugi strani pa lahko eksosomi interagirajo z zdravimi celicami, prenašajo svoj toksični tovor in širijo patološke spremembe 10. Rajendran in sodelavci so na primer pokazali, da eksosomi, ki izvirajo iz nevronov, pospešujejo združevanje in/ali razpad beljakovin Aβ in proteinov tau, ki so odgovorni za nastanek amiloidnih plakov, značilnih za napredovanje Alzheimerjeve bolezni 13.
Zunajcelični vezikli omogočajo prenos tovora preko KMP
Idealni scenarij za vnos zdravil do tarče je, da zdravilo spravimo na mesto učinkovanja, tam v bioaktivni koncentraciji deluje na obolele celice (»jih ozdravi«) lokalno, pri tem pa sočasno ne povzroča škode ali sistemskih stranskih učinkov. Vektorji prenosa morajo biti navadno konjugirani z biološko prepoznavno enoto, ki se lahko veže na površino ciljne celice. Težava je v tem, da se ciljni receptorji konjugiranega liganda navadno ne nahajajo zgolj na tarči, temveč tudi na zdravem tkivu. Eksosomi, ki se izločajo iz različnih celic, pa so selektivno usmerjeni in jih torej predhodno ni potrebno manipulirati, da bi dosegli specifičnost njihovega delovanja. Predstavljajo idealne vektorje za prenos bioloških molekul do tarče, saj so telesu lastni, niso citotoksični, so ciljno specifični in lahko prehajajo preko bioloških preprek ter tako omogočajo personaliziran pristop k zdravljenju 11.
Številne študije nakazujejo, da lahko zunajcelični vezikli iz perifernih endotelijskih celic prečkajo KMP in prenesejo vsebino v CŽS. Iz tega izhaja ideja, da bi jih uporabili kot prenašalce za prenos bioloških molekul ali zdravil preko KMP. Alvarez-Erviti in sodelavci so z uporabo avtolognih eksosomov dendritičnih celic pri miših za vnos molekule siRNA BACE1 (beta-sekretaza 1, encim, ki sodeluje pri tvorbi mielinskih ovojnic in je povezan z nastankom Alzheimerjeve bolezni pri mišjem modelu) dosegli znižanje regulacije proteina BACE1. S poskusom so potrdili, da lahko eksosome uporabimo kot varno in učinkovito orodje za neinvaziven vnos molekul preko KMP, hkrati pa ne sprožimo imunskega odziva 14. V drugi študiji so Zhuang in sodelavci v eksosome vključili molekule inhibitorja, ki je upočasnil rast tumorja, za vnos pa uporabili intranazalno pot injiciranja 15. Pri mišjem modelu Parkinsonove bolezni so Cooper in sodelavci v eksosome z vezanim peptidom RVG (angl. Rabbies Virus Glycoprotein), ki se ciljno veže na nevralne celice in endotelijske celice v možganih in pozitivno vpliva na prehajanje KMP, vključili molekule siRNA za regulacijo gena za α-sinukelin. Agregati α-sinukelina so glavne sestavine Lewijevih telesc, poglavitne patološke možganske spremembe Parkinsonove bolezni. Z vnosom molekule siRNA so raziskovalci zmanjšali vsebnost celokupnega in agregiranega α-sinukelina v mišjih možganih in pokazali, da je pod določenimi pogoji mogoče upočasniti patološke spremembe 16.
Eksosomi kot terapevtsko orodje za zdravljenje bolezni CŽS
Ker eksosomi lahko prehajajo KMP, se preučujejo številni pristopi za zdravljenje bolezni CŽS z eksosomi kot terapevtskimi vektorji. Naštetih je nekaj najpogosteje uporabljenih pristopov:
Terapevtske aplikacije z uporabo nespremenjenih eksosomov. Eksosomi sami po sebi vsebujejo zelo raznolik tovor (odvisno, od kje izvirajo) in imajo v primerjavi s progenitorsko celico prehoden učinek na ciljne celice, kar jih naredi bolj varne. Terapevtsko delovanje multipotentnih mezenhimskih matičnih celic je na primer odvisno od njihovega sekretoma, ta pa poleg eksosomov vsebuje še druge molekule, ki lahko negativno vplivajo na ciljno tkivo.
Vnos terapevtskih učinkovin v nespremenjene eksosome. Gre za poseben pristop, saj je potrebno učinkovino vnesti v eksosome tekom same biogeneze. Biomolekule ali zdravilne učinkovine mora najprej ponotranjiti progenitorska celica, to pa dosežemo tako, da jih inkubiramo skupaj pod definiranimi pogoji. Izločeni eksosomi vsebujejo želeno molekulo, trenutno največji izziv pa je doseči dovolj veliko količino izločenih eksosomov z vsebovano učinkovino. Drug način je, da učinkovino vnesemo v že izolirane eksosome – s pasivno inkubacijo ali aktivnimi načini vnosa (elektroporacija, tretiranje z detergenti ali ultrazvokom).
Eksosomi in vnos farmacevtskih učinkovin. Ta način je za raziskovalce posebno zanimiv v povezavi s prehajanjem KMP. Gre za pasiven vnos zdravil in dostavo do ciljnega mesta v CŽS preko KMP. Zanimiva je možnost uporabe intranazalne poti vnosa v CŽS, ki je direkten in preko katerega se izognemo zadrževanju veziklov v obtočilnem sistemu.
Eksosomi kot sistem za prenos proteinov. Če v progenitorske celice z uporabo plazmidov vnesemo zapis za izbrani protein, lahko izločeni eksosomi vsebujejo sam protein ali genetski zapis za tvorbo proteina in to prenesejo do ciljnih celic. Pomemben vidik so tudi površinsko vezani proteini, npr. antigen-predstavitvene molekule, ki omogočajo potovanje ekosomov na določeno mesto in regulacijo imunskega sistema.
Eksosomi kot sistem za prenos nukleinskih kislin. Metoda je uporabna za prenos regulatornih molekul RNA, ki jih ciljna celica lahko ponotranji. Tako molekula RNA lahko vpliva na povišano ali znižano regulacijo genov ciljne celice. Na poti do cilja jih eksosomi ščitijo pred delovanjem zunajceličnih endonukleaz 4 10 17.
Zaključek
Zunajcelični vezikli, predvsem eksosomi, kot terapevtsko orodje predstavljajo zanimivo raziskovalno področje, tudi zaradi njihove pomembne vloge v medcelični komunikaciji. Eksosomi, ki jih izločajo možganske celice, lahko pomembno vplivajo na mikrookolje in prispevajo k napredovanju bolezni ali pa delujejo daljnosežno s prenosom preko bioloških tekočin. Te njihove izjemne lastnosti nam omogočajo, da jih uporabljamo kot biološke označevalce ali kot prenašalce bioloških molekul in zdravil na ciljna mesta. Ko bomo natančno poznali mehanizme njihovega delovanja ter jih znali učinkovito izolirati in/ali modificirati, se nam bodo odprle številne možnosti uporabe, tudi prepotreben razvoj novih metod zdravljenja bolezni centralnega živčnega sistema.
-
___
-
Dong H. Current strategies for brain drug delivery. Theranostics. 2018;8:1481-1493. ↩
-
Wood MJA, O’Loughlin AJ, Samira L. Exosomes and the blood-brain barrier: implications for neurological diseases. Therapeutic Delivery. 2011;2:1095-1099. ↩
-
World Health Organization. The top 10 causes of death. World Health Organization. https://www.who.int/news-room/fact-sheets/detail/the-top-10-causes-of-death. Objavljeno maja 2018. Datum dostopa 07.07.2020. ↩
-
Aryani A, Denecke B. Exosomes as a nanodelivery system: a key to the future of neuromedicine? Molecular neurobiology. 2016;53:818-834. ↩
-
Hersh DS, Wadajkar AS, Roberts N. Evolving drug delivery strategies to overcome the blood brain barrier. Current pharmaceutical design. 2016;22:1177-1193. ↩
-
Andras IE, Toborek M. Extracellular vesicles of the blood-brain barrier. Tissue Barriers. 2016;4:e1131804. ↩
-
Gray SJ, Woodard KT, Samulski RJ. Viral vectors and delivery strategies for CNS gene therapy. Therapeutic delivery. 2010;1:517-534. ↩
-
Saraiva C, Praca C, Ferreira R. Nanoparticle-mediated brain drug delivery. Overcoming blood-brain barrier to treat neurodegenerative diseases. Journal of controlled release. 2016;235: 34-47. ↩
-
Rufino-Ramos D, Albuquerque PR, Carmona V. Extracellular vesicles: novel promising delivery systems for therapy of brain diseases. Journal of controlled release. 2017;262:247-258. ↩
-
Thery C, Zitvogel L, Amigorena S. Exosomes: composition, biogenesis and function. Nature reviews immunology. 2002;2:569-579. ↩
-
Barile L, Vassalli G. Exosomes: therapy delivery tools and biomarkers of disease. Pharmacology and therapeutics. 2017;174:63-78. ↩
-
Sun D, Zhuang X, Zhang S. Exosomes are endogenous nanoparticles that can deliver biological information between cells. Advanced drug delivery reviews. 2013;65:342-347. ↩
-
Rajendran L, Honsho M, Zahn TR. Alzheimer’s disease β-amyloid peptides are released in association with exosomes. Proceedings of the national academy of sciences. 2006;103:11172-11177. ↩
-
Alvarez-Erviti L, Seow Y, Yin H. Delivery of siRNA to the mouse brain by systemic injection of targeted exosomes. Nature Biotechnology. 2011;29:341-345. ↩
-
Zhuang X, Xiang X, Grizzle W. Treatment of brain inflammatory diseases by delivering exosome encapsulated anti-inflammatory drugs from the nasal region to the brain. Molecular therapy, the journal of the american society for gene therapy. 2011;19:1769-1779. ↩
-
Cooper MJ, Wilander OPB, Nordin JZ. Systemic exosomal siRNA delivery reduced alpha-synuclein aggregates in brains of transgenic mice. Movement disorders. 2014;29:1476-1485. ↩
-
Ha D, Yang N, Nadithe V. Exosomes as therapeutic drug carriers and delivery vehicles across biological membranes: current perspectives and future challenges. Acta Pharmaceutica Sinica B. 2016;6:287-296. ↩
dr. Saša Koprivec, univ. dipl. bioteh.
Laboratorij za genomiko
Inštitut za predklinične vede
Veterinarska fakulteta UL